11月4日,貝達藥業CFT8919膠囊Ⅰ期臨床研究完成首例受試者入組。該研究名為“評價CFT8919膠囊在局晚期或晚期轉移性非小細胞肺癌患者中的安全性、 耐受性、藥代動力學特征和抗腫瘤活性的Ⅰ期臨床研究”。牽頭單位為浙江省腫瘤醫院,主要研究者為范云教授。
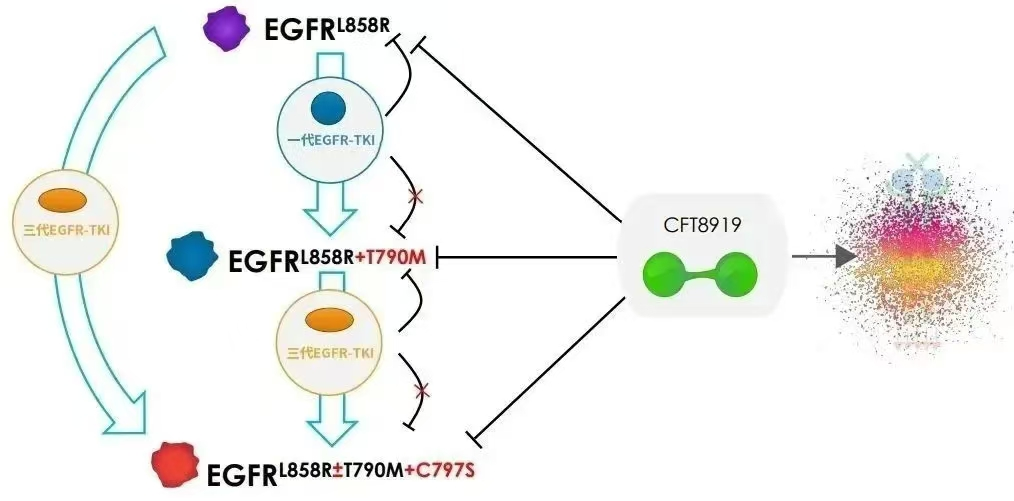
△CFT8919作用機理圖(來源:C4T)
本研究包括劑量遞增研究、劑量擴展研究和隊列擴展研究,主要目的是評價CFT8919膠囊在局晚期或晚期轉移性NSCLC中的安全性和耐受性以及評價CFT8919膠囊在不同NSCLC隊列中的抗腫瘤活性。
CFT8919 是一種針對EGFR-L858R的可口服的選擇性變構雙功能降解活性化合物。臨床前體外實驗證實CFT8919 對多種攜帶 L858R突變的EFGR 蛋白具有良好的降解能力,同時對像T790M或C797S突變的EGFR繼發耐藥突變有效。另外在體外模型中,CFT8919具有較好的腦穿透,具有預防或治療患者腦轉移的潛力。
浙江省腫瘤醫院范云教授表示, 肺癌是我國發病率和死亡最高的惡性腫瘤,目前EGFR突變的非小細胞肺癌患者在三代EGFR-TKI使用之后依然避免不了耐藥,迫切需要開發具有不同作用機制的藥物來克服耐藥以改善患者的預后。尤其對于攜帶EGFR-L858R突變非小細胞肺癌患者預后相對較差,臨床上仍存在較大的未滿足需求,亟需更好的治療方案。CFT8919是一款針對EGFR-L858R 突變的蛋白降解劑,期待該藥物研究順利開展,早日獲批,為EGFR突變耐藥患者帶來新的希望。
貝達藥業副總裁張惠軍表示, CFT8919臨床前藥效研究數據表明對多種攜帶 EGFR-L858R突變的EFGR 蛋白具有良好的降解能力,能夠顯著抑制多種攜帶L858R單突變、雙突變、三突變,同時選擇性高,不誘導野生型EGFR蛋白的降解。臨床前藥代及毒理學研究數據也表明CFT8919作為抗腫瘤藥物,可以進入到臨床開發階段。我們也期待臨床研究的順利開展,相信在研究中心和專家的推進下,能夠早日進入關鍵臨床,惠及患者。
關于CFT8919
2023年5月貝達藥業與C4 Therapeutics (C4T)公司宣布就CFT8919項目達成戰略合作,貝達藥業取得在中國(包括香港、澳門和臺灣地區)開發、制造和商業化CFT8919的權利,并可獲得前述區域以外約定比例的銷售提成。
關于C4 Therapeutics
C4 Therapeutics (C4T)是一家致力于靶向蛋白質降解科學研究的生物制藥公司,專注創造改變患者生活的新一代藥物。C4T正在利用其TORPEDO?平臺有效地設計和優化小分子藥物,利用人體的天然蛋白質回收系統快速降解致病蛋白質,從而有可能克服耐藥性。
下一條: 貝達藥業攜手瑞普晨創 共拓細胞治療新賽道
